Santhera 10月26日宣布,已获得美国食品药品管理局(以下简称 "FDA")批准,将Agamree®(伐莫洛龙)40 mg/mL口服混悬液用于治疗两岁及以上的杜氏肌营养不良症(以下简称 "DMD")患者。Agamree 为 DMD 提供了一种新型皮质类固醇治疗方案,满足了尚未得到满足的重大医疗需求。2023 年 7 月,Catalyst 从 Santhera 公司获得了 Agamree 用于 DMD 和其他潜在适应症的北美独家许可和商业权利,通过一项高度协同的神经肌肉资产增强了其神经科学商业产品组合。作为交易的一部分,Santhera 将立即把 Agamree 已获批准的新药申请转让给 Catalyst。
FDA 批准 Agamree® 的依据是关键的 2b 期 VISION-DMD 研究数据,以及从三项开放标签研究(包括延长研究)中收集的安全性信息。在这些试验中,Agamree 的用药剂量为 2 至 6 毫克/千克/天,疗程长达 48 个月。与目前的标准皮质类固醇疗法相比,这种新型皮质类固醇疗法的疗效相当,数据表明不良反应有所减少,尤其是与骨骼健康、生长轨迹和行为有关的不良反应。
Agamree 已获得美国 DMD 孤儿药和罕见儿科疾病认定资格,自批准之日起将有资格获得 7 年的孤儿药专营权,并已获得可提供保护至 2040 年的待批专利。
关于杜兴氏肌肉萎缩症 (DMD)
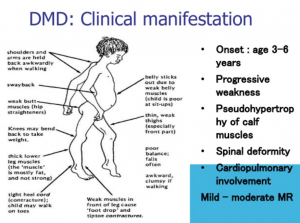
杜兴氏肌肉萎缩症(DMD)是最常见的肌肉萎缩症,是一种罕见的危及生命的神经肌肉疾病,其特点是进行性肌肉功能障碍,最终导致丧失行动能力、呼吸衰竭和死亡。目前治疗 DMD 的标准方法是使用皮质类固醇,但往往会产生严重的副作用。据估计,美国有 11,000 到 13,000 名 DMD 患者,其中约 70% 的患者目前同时接受皮质类固醇治疗。
关于 Agamree®(vamorolone)
Agamree 的独特作用模式基于对糖皮质激素和矿质皮质激素受体的不同作用,以及对进一步下游活性的改变,因此被认为是一种新型皮质类固醇,在维持疗效方面具有分离特性,同时具有更好的副作用耐受性。这种作用机制可能使瓦莫罗隆成为当前标准疗法皮质类固醇的有效替代品,适用于儿童、青少年和成年 DMD 患者。在关键的 VISION-DMD 研究中,vamorolone与安慰剂相比,在治疗 24 周时达到了主要终点 "站立时间 (TTSTAND) 速度"(p=0.002),并显示出良好的安全性和耐受性。与安慰剂相比,VISION-DMD 研究中最常报告的不良事件是库欣样特征、呕吐和维生素 D 缺乏。不良反应的严重程度一般为轻度至中度。
内容来自中国SFDA,美国FDA,药品审评中心、国家基本医保目录等权威部门,部分内容来自互联网,如涉及医学知识、观点、建议都不应被视为医生建议或处方诊断,所有信息仅供参考,康和医药不对其承担任何责任,如有错误,版权问题请来电来函告知。